转座子的类型和作用机制(两种定义及使用机制)

在我们研究某种疾病的发病机制或者某种药物的作用靶点时,经常需要建立目的基因过表达或基因敲除的细胞模型,目前构建稳转细胞株及部分敲除细胞株最常用的方式之一是慢病毒法,慢病毒因其可以转染几乎所有种类的细胞,且在转染后可以整合到细胞的基因组而长期表达的优势,是目前较为主流的构建方法,但慢病毒构建的稳转细胞株相对于野生型没有生长优势;此外,慢病毒对目的基因的载量也有限。因此,寻找一种高效简便可替代慢病毒法的方法显得尤为重要。
转座子的出现为构建基因编辑细胞株提供了一个全新的视野。转座子也被称为跳跃基因,由Barbara McClintock教授在上世纪50年代发现,并于1983年因此发现而获得诺贝尔医学奖,是指一段DNA序列由基因组的一个位置跳跃到另一个位置。转座子主要包含两种类型:
? 一类转座子:逆转座子(retrotransposons),自身不表达转座酶,先转录为RNA,通过RNA的反转录获得cDNA,cDNA在整合酶的作用下转移到其他基因组位置。
? 二类转座子:DNA转座子(DNA transposons),通过自身编码的转座酶直接切割转座子所在DNA序列,实现序列的转移。在脊椎动物中发现的转座子系统中,以睡美人转座子(SleepingBeauty)和piggyBac转座子等DNA转座子最为常见。
睡美人转座子是由科学家Levis于1997年在脊椎动物中首个发现的转座子, 其通过生物信息学方法分析8种鲑鱼中12个Tc1类转座酶序列,找出了其中的保守序列,确定了已经灭绝的鲑鱼中具有活性的转座酶的基因序列,并称其为睡美人转座子。但睡美人转座子对宿主要求严格,且存在转座效率不稳定等情况,限制了其广泛应用,而piggyBac转座子则因其特异的整合位点、精密切割以及广泛存在的特性被大家所青睐。
PiggyBac转座子结构与机制
PiggyBac转座子(粉纹夜蛾)是一个2475bp长的可自主转移元件,两末端分别有一个由13bp和19bp的TIR序列组成的亚末端重复序列,两端TIR序列之间的间隔分别是3bp(5’端)和31bp(3’端),在两个亚末端重复序列之间,有一个1.8kb的开放阅读框,编码由594个氨基酸组成、分子量大小为64KD的PiggyBac转座酶。如下图所示:
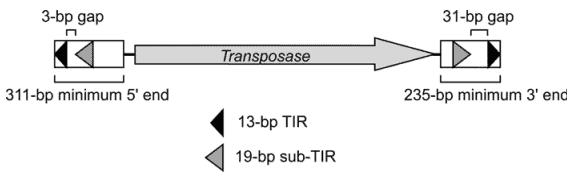
PiggyBac属于II类转座子,通过“剪切-粘贴”机制移动,即从基因组一个位置转座到另一个位置,不留下序列本身(与I类启动子通过“复制-粘贴”的移动方式不同)。
通过对PiggyBac超家族成员序列比对结果分析,发现PiggyBac转座酶保守的氨基酸位点为D268、D346和D447,与许多其它的转座酶和逆转录酶的保守结构域DDE类似,这三个位点参与了几乎所有的转座活动,包括DNA切割、发夹结构形成和目的序列的插入。具体的整合过程如下图所示:
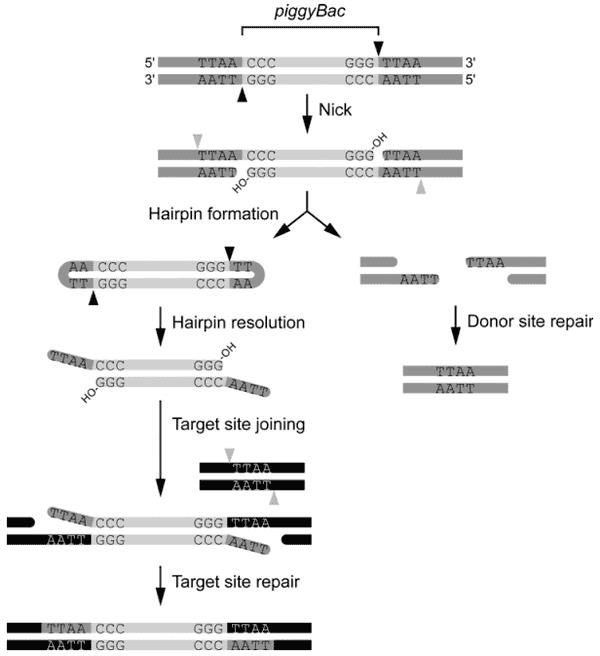
PiggyBac转座酶结合到转座子DNA序列两端,开始精确地切割每条DNA链转座子DNA的3’端,形成3’-OH结构;之后3’-OH攻击互补链5’末端TTAA与转座子间的磷酸二酯键,导致互补链DNA断裂,释放转座子,同时转座子两端形成发夹结构;找到新的TTAA四碱基整合位点后,转座酶伸展转座子的发夹结构,暴露3’-OH,同时3’-OH攻击TTAA整合位点的5’端,形成新的磷酸二酯键;互补链及转座子释放位点处的单链缺口的修复由宿主因子完成,转座完成。
PiggyBac转座子载体系统组成
PiggyBac转座子在发现后经过了一系列优化和改造的过程,如转座酶密码子优化,以及两端TIR序列的简化,最后形成了一套完整的PiggyBac载体系统。PiggyBac载体系统成员主要有:一个辅助质粒:编码转座酶;一个转座子质粒:含优化的两端亚末端反向重复序列,中间是被转座区域,可插入我们想转座到宿主基因组中的目的基因序列。
实验时需同时将辅助质粒和转座子质粒共同转化靶细胞,辅助质粒编码的转座酶识别转座子质粒两端的TIR序列并切割,释放的被转座区被转座酶整合到宿主基因组中含TTAA序列的位点,并在被转座区两端出现TTAA重复序列。
在不降低转座效率的情况下,两端优化后的TIR序列间可插入10kb左右的序列,研究表明,在小鼠中通过受精卵注射的方式,用PiggyBac转座子载体在基因组插入细菌人工染色体(BACs,150kb-300kb),转座效率最高的达到了45%(F0代中有45%的小鼠携带了BACs)。
应用
1. 作为非病毒载体
与传统的病毒载体相比,PiggyBac具有以下几大优点:首先是安全性高、操作方便(可直接用质粒转化细胞);其次是载体容量大(10kb-20kb),可实现多基因的共表达;第三是可通过调节转座子质粒和辅助质粒的比例,提高外源基因的整合效率,并且可通过反向PCR精确确定目的基因插入的位置;第四是再次转座后实现精确切离;第五是转座后不引起染色体重排等不稳定现象;最后是宿主范围广,转座效率高,较少依赖宿主因子。
2. 基因治疗
研究表明,PiggyBac转座系统在Hela、HEK293、CHO及H1299等细胞中高效转座,且携带的目的基因稳定表达,因而是很有吸引力的基因治疗候选载体之一。
3. 突变工具
PiggyBac再次转座偏向插入基因内部且插入位点分布较广,可用作基因插入突变的工具,这点为哺乳动物的基因组功能研究提供了较好的研究工具。
赛业OriCell目前已应用PiggyBac与基于传统CRISPR/Cas9研发而成的CRISPR-Pro技术结合实现大片段基因敲除,与移码突变相比,敲除更彻底,各项实验数据表明采用CRISPR-Pro技术更高效。相比于传统病毒法构建的细胞株,使用PiggyBac构建的细胞株具有更高的遗传稳定性。赛业OriCell扎根基因敲除领域14年,拥有上万例基因敲除项目经验,平台成熟稳定,目前已成功敲除细胞株种类超过198种,成功保障,安全无忧。